CompanyNews
CompanyNews
Media | CompanyNews 11404 Views 2020-03-25 09:00
本文由医药魔方Pro团队授权转载
近日,来自德克萨斯大学M.D.安德森癌症中心等机构的研究人员公布了美国首个CAR-NK细胞临床试验(NCT03056339)的结果。研究显示,用脐带血来源的CAR-NK疗法治疗既往接受过大量治疗的复发或难治性非霍奇金淋巴瘤(NHL)和慢性淋巴细胞白血病(CLL)患者后,大多数患者产生了临床响应,且未出现主要的毒性作用。相关数据发表于顶级医学期刊NEJM杂志上[1]。
具体来说,研究者们从捐赠的脐带血中分离出NK细胞,经过逆转录病毒载体转导相关基因使NK细胞表达理想的嵌合抗原受体(CAR),用以识别癌症特异性抗原(在该研究中为CD19)。该研究中使用的NK细胞经过改造还能够表达用于增强NK细胞在体内扩增和存活的细胞因子白细胞介素15和一种起安全开关作用的酶—— 可诱导型caspase 9。
11例患者(5例CLL患者、6例NHL患者)在淋巴细胞清除性化疗后接受单剂脐带血来源的CD19 CAR-NK细胞治疗,以三种剂量(1×105、1×106或1×107 CAR-NK细胞/kg体重)之一给药。前9例患者接受CD19 CAR-NK细胞治疗前进行了人类白细胞抗原(HLA)匹配,但最后两例患者未进行HLA匹配。
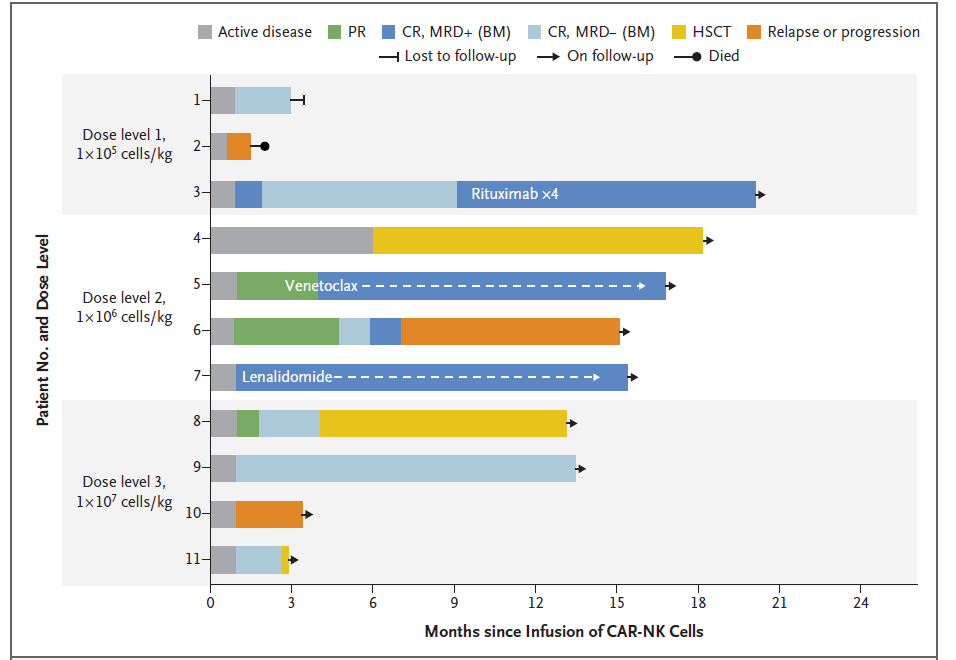
CAR-NK疗法的临床响应和缓解后治疗(来源:NEJM)
疗效方面,参与研究的11例患者中,有8例(73%)在接受治疗30天内响应CD19 CAR-NK疗法,中位随访13.8个月后,8例患者中有7例(3例CLL、4例NHL)获得完全缓解(CR),不再显示疾病迹象。不过,需要指出的是,在接受CAR-NK治疗后达到缓解的8例患者中,有5例接受了缓解后治疗。
安全性方面,没有患者出现细胞因子释放综合征(CRS)或神经毒性。治疗后包括IL-6在内的炎性细胞因子水平未增加。此外,尽管使用了供者细胞,也没有发生移植物抗宿主病。
持久性方面,所有剂量水平的CAR-NK细胞在被回输到患者体内一个月内均反应明显,且在回输至少一年后依然在患者体内以低水平存在。
生产方面,与自体CAR-T疗法不同(需要使用患者自己的T细胞进行基因改造,生产过程需要数周),由于该研究中使用的CAR-NK细胞是同种异体的,即细胞来源于健康供者,因此有望实现提前生产并存储起来,以便需要时可立即使用。此外,1例供者的脐带血可生产出用于多例患者的CAR-NK产品。
总结来说,这些数据和信息表明,在针对CD19阳性血癌患者的I/II期临床试验中,CAR-NK细胞疗法显示出了安全性和有效性。这一令人鼓舞的初期结果支持开展进一步的临床研究,调查同种异体脐带血来源的CAR-NK细胞能否作为癌症患者的治疗选择。

CAR-NK是继CAR-T之后最令人期待的工程细胞疗法之一。基于NEJM报道的这些数据,有几个问题引人深思,如CAR-NK毒性非常低的可能原因是什么?除了健康供者脐带血,CAR-NK还有哪些来源?除了CD19,可用于开发CAR-NK的靶点还有哪些?在治疗实体瘤方面,CAR-NK是否与CAR-T一样困难?CAR-NK还有哪些方面需要优化?

近日,带着这些疑问,医药魔方Pro采访了国内早在2014年就已率先布局CAR-NK疗法的博生吉公司的董事长杨林教授。杨林教授在采访中表示,M.D.安德森癌症中心所获得的这些数据表明,CAR-NK细胞具有成为一种现货型(off-the-shelf)同种异体细胞治疗的强大潜力,在不久的将来很有可能成为CAR-T治疗的一大竞争对手。
以下是采访实录:
医药魔方Pro:首先,能否请您点评一下NEJM公布的这些数据?
杨林教授:从2017年两款CD19 CAR-T细胞治疗产品Yescarta和Kymriah获批上市以来,肿瘤细胞治疗一直都是以患者自体免疫细胞为主要原材料,经体外活化、基因修饰、扩增培养之后再回输至患者体内。这种细胞制备方式主要有三大问题:(1)以患者自身T细胞为原材料,其品质不一,制备时容易有失败风险;(2)自体CAR-T制备时间较长(含质控约14天左右),某些疾病进展较快的患者无法等待这么长时间;(3)由于每一份细胞都需要一套完整的制备和质控流程,因此价格非常高昂(美国约为40万美元左右)。为了解决这些问题,发展同种异体细胞治疗产品成为这两三年内肿瘤免疫细胞治疗领域的主要方向之一。
在这篇NEJM中,11例接受异体CD19 CAR-NK细胞回输治疗的患者中,有8例(73%)达到客观缓解(OR),其中7例患者达到完全缓解(CR),其疗效并不亚于市面上的CD19 CAR-T细胞治疗产品。除此之外,CAR-NK细胞毒副作用较低,在所有患者中都没有看到CAR-T细胞治疗常见的细胞因子风暴(CRS)及神经毒性副作用;即使在HLA完全不匹配时,也没有造成移植物抗宿主病(GvHD)的情形。此外,从脐血来源制备的CAR-NK细胞,每批次能生产超过100人份的剂量,生产成本比起CAR-T细胞大幅降低。综合以上优势,这篇文献的数据证明,CAR-NK细胞具有成为一种现货型(off-the-shelf)同种异体细胞治疗的强大潜力,在不久的将来很有可能成为CAR-T治疗的一大竞争对手。
医药魔方Pro:NEJM报道的试验中,CAR-NK显示的毒性非常低,您认为可能的原因是什么?
杨林教授:我认为,CAR-NK毒性较低的原因,主要与细胞本身不容易导致过高的细胞因子分泌有关。CAR-T治疗最常见的毒副作用为细胞因子风暴(CRS),其主要是由于IL-6升高所导致。NEJM的这篇论文也提到,CAR-NK受试者的IL-6浓度均处于较低的水平;CAR-T治疗另一个常见的副作用则是神经毒性,有报道指出这类神经毒性的产生与IL-1的分泌较为相关,不过NEJM报道的这项试验似乎没有检测IL-1的浓度,因此无法明确判断是否CAR-NK也产生较低的IL-1因子。
医药魔方Pro:除了使用健康供者脐带血,CAR-NK还有哪些来源?
杨林教授:首先,以原代细胞来说,除了NEJM这篇论文中提到的健康供者脐带血之外,NK/CAR-NK细胞治疗的细胞来源还有健康供者周边血液以及产后的胎盘组织。
另外,由于NK肿瘤细胞株NK-92也展现出了与正常NK细胞类似的细胞杀伤活性,许多NK-92及CAR-NK-92产品目前也处于临床测试阶段,不过这类产品由于安全性的因素,在生产过程中须经过辐照处理以消除其体内扩增能力,从目前已经公布的临床数据来看,似乎疗效有限。
除上述细胞来源之外,人类多能干细胞,比如脐血来源的造血干细胞以及诱导性多能干细胞(iPSC),都已经成功被诱导成NK细胞,并具有良好的细胞杀伤能力。由于干细胞可以提供无限生长且品质均一稳定的细胞来源,所以被视为最具潜力的细胞治疗产品来源。去年,美国Fate Therapeutics公司经诱导性多能干细胞(iPSC)分化而得的NK细胞(FT500)已正式进入I期临床,第二个改良型的NK产品(NK516)也在去年底获得IND批准,相信不久的将来,iPSC来源的CAR-NK细胞也会很快进入临床测试阶段。
医药魔方Pro:目前,可用于开发CAR-NK的靶点有哪些?这些靶点是如何选择的?
杨林教授:目前已经用于CAR-T细胞上的靶点,如CD19、BCMA、以及其他靶点等,都可以用在CAR-NK治疗上,所以在靶点选择策略上,CAR-T和CAR-NK是非常类似的。NEJM报道的这项试验之所以选择CAR-T最常见的CD19作为第一个靶点,也算是一种proof-of-concept的做法,可以有效地比较CAR-T和CAR-NK的不同,据我所知,M.D.安德森癌症中心同一研究团队的BCMA-CAR-NK项目也在加速开展中。
值得一提的是,我认为,与CAR-T在治疗B细胞癌症方面临床疗效显著不同,CAR-NK细胞对于治疗T细胞恶性肿瘤相关适应症(比如:急性 T 淋巴细胞白血病及T淋巴母细胞淋巴瘤)是非常有优势的。对于使用CAR-T细胞来治疗T细胞恶性肿瘤来说,主要有两大瓶颈:(1)若使用患者自体CAR-T细胞治疗时,容易有肿瘤T细胞污染的问题;(2)不论自体或异体回输,使用T细胞作为原材料时,必须提前利用基因编辑或其他策略去除T细胞自身表面上的靶点,否则在转染CAR之后会有CAR-T细胞自杀(fratricide)的问题。而使用异体回输的CAR-NK细胞则可以有效避免这两点问题,因此若要开展CAR-NK项目,我建议优先应用于T细胞恶性肿瘤这类适应症上。
医药魔方Pro:在治疗实体瘤方面,CAR-NK是否也面对与CAR-T一样的难题?
杨林教授:是的,实体瘤治疗的主要困难点之一在于肿瘤的异质性(heterogeneity),因此,无论是CAR-T或CAR-NK,单一靶点的CAR免疫细胞都无法完全清除所有的实体肿瘤细胞;另外一个实体瘤治疗的瓶颈则在于肿瘤微环境(tumor microenvironment,TME),先前的报道指出,TME同样也会造成NK细胞在肿瘤内部缺氧、营养不足和代谢失调的情况。总结以上两点,我认为要克服实体瘤的困难,不论是CAR-T或CAR-NK都还需要进一步改造,或者利用与其他药物联用的方式,来达到更好的肿瘤清除效果。
医药魔方Pro:博生吉是何时开始启动CAR-NK研发的?研发过程中有没有遇到什么困难?
杨林教授:博生吉自2014年就开始启动CAR-NK的研发工作。不过当时采用的技术路线与Nantkwest公司类似,是以NK92细胞为效应细胞来进行CAR-NK的制备。在成功建立了大规模制备工艺的基础上,我们开展了针对实体肿瘤和血液肿瘤的POC临床研究工作,取得了一些成绩。不过NK92细胞存在诸多限制,除了前面提到的需要辐照处理之外,还包括体内存活时间极短,大约只能存活3天左右,因此需要重复多次给药;此外,NK92细胞在体内没有扩增能力。因此以NK92细胞为基础开展的CAR-NK治疗,由于失去了细胞药物实现临床疗效最关键的体内扩增与持续性两个关键属性,其临床疗效大打折扣。再加上多次重复给药和高剂量给药的要求,也急剧增加了治疗成本。临床新药的开发,治疗疗效是基本要求,如果基于NK92的CAR-NK产品其疗效无法与CAR-T竞争,那么这样的产品竞争力和生命力就会很差。鉴于这样的情况,博生吉在2017年就暂停了基于NK92细胞的CAR-NK研发。不过异体现货型细胞产品仍然是博生吉的追求目标,因此博生吉正在积极开发更具竞争力和生命力的异体现货型细胞疗法——CAR-γδT,并取得了可喜的进展,目前正在启动POC临床试验和IND申报的准备工作。
医药魔方Pro:您认为,目前CAR-NK还有哪些需要优化的方面,或者还有哪些难题需要克服?
杨林教授:就NEJM报道的研究结果来看,我认为,的确有些内容是研究者还需要进一步探索的。第一,此临床试验中的11例患者均使用新鲜回输的NK细胞,若想真正成为一种现货型的产品,研究者还需确认冻存后的细胞是否可以达到相同的疗效;第二,研究者预估CAR-NK细胞和CAR-T细胞都可能会有肿瘤复发的可能,所以此临床研究允许在主治医师的决定下使用其他治疗,以确保患者达到有效缓解,但也由于这个原因,单独使用CAR-NK治疗时的疗效持续时间,在本研究中没有得到明确的评估;除此之外,11例患者中,有9例患者使用的CAR-NK细胞的HLA配型是部分相配(4 of 6 matches at HLA loci A, B, and DRβ1)的,仅有2例患者没有考虑配型问题,因此我认为CAR-NK治疗是否可以完全不考虑HLA配型,可能还需要入组更多的患者再做进一步确认。
医药魔方Pro:最后,总体来说,您如何看待CAR-NK的前景?是否比CAR-T更令人期待?
杨林教授:综合NEJM报道的数据和信息,脐血来源的CAR-NK细胞产品较目前市面上的自体CAR-T细胞治疗具有许多优势,主要包括:成本较低、患者无须等待制备时间、毒副作用较低等等。因此如果这个CAR-NK细胞产品将来能成功获批上市,对于市场冲击将会是非常巨大的。这些优势将会一直存在,直到新一代的细胞治疗产品(例如:干细胞来源的免疫细胞疗法)上市为止。也因此,我认为企业必须不断地创新求变,开展新靶点、新适应症,新产品的研发,才能在这个瞬息万变的细胞治疗市场中生存及发展。
相关论文:
[1] Enli Liu et al. Use of CAR-Transduced Natural Killer Cells in CD19-Positive Lymphoid Tumors. NEJM(2020).
参考资料:
1# CD19 CAR NK-cell therapy achieves 73% response rate in patients with leukemia and lymphoma(来源:University of Texas M.D. Anderson Cancer Center)
2# CAR Natural Killer Cell Therapy Safe and Effective in First Trial (来源:JAMA)
3# 应用CAR转导的自然杀伤细胞治疗CD19阳性淋巴肿瘤(来源:NEJM)
4# Engineered natural killer cells may be the next great cancer immunotherapy (来源:Science)